ARTICULO
Enero 02, 2024
Modelo de consulta compartida
ARTICULO
Enero 01, 2024
ARTICULO
Enero 01, 2024
ARTICULO
Enero 01, 2024
ARTICULO
Octubre 21, 2023
ARTICULO
Enero 02, 2022
ARTICULO
Octubre 18, 2020
Categorías
Dentro de este apartado incluiremos las diferentes aportaciones, protocolos, técnicas, etc.… que nos permitan el diagnostico de las diferentes enfermedades y que forma parte de la ayuda rápida en la consulta.
Dentro de este apartado incluiremos las diferentes aportaciones, protocolos, técnicas, etc.… que nos permitan el tratamiento de las diferentes enfermedades y que forma parte de la ayuda rápida en la consulta.
Dentro de este apartado incluiremos las diferentes aportaciones, protocolos, técnicas, etc.… que nos permitan el control, prioritariamente a largo plazo, de las diferentes enfermedades y que forma parte de la ayuda rápida en la consulta.
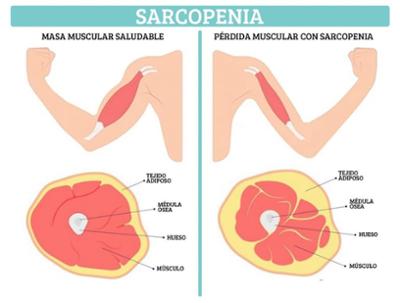
Dentro de este apartado incluiremos, prioritariamente de manera visual, de técnicas que nos permitan el diagnostico de las diferentes enfermedades y que forma parte de la ayuda rápida en la consulta.
Dentro de este apartado incluiremos las diferentes aportaciones, protocolos, técnicas, etc.… que nos permitan la prevención y profilaxis de las enfermedades y que forma parte de la ayuda rápida en la consulta.
Últimas entradas
ARTICULO
Marzo 10, 2024
ARTICULO
Febrero 20, 2024
ARTICULO
Enero 25, 2024
ARTICULO
Enero 02, 2024